臓器移植後の患者さんの自由な生活のために
免疫寛容プロジェクトは、移植後の患者さんにもっと自由な生活を、免疫抑制剤を必要としない未来を届けたいという医師の願いからスタートしました。
臓器移植は、従来の方法では治療することが出来ない臓器不全に対する究極の治療法として普及してきました。移植医療の発展は、拒絶反応を抑える免疫抑制剤に支えられてきました。しかし同時に、生涯服用する免疫抑制剤の副作用は大きな問題となっています。ウイルス等への感染が起こりやすくなる他、長期間の服用に伴い癌の再発、心疾患や腎機能などへの影響も報告されています。そのため、移植後も患者さんの生活は、多くの制限を受けてしまいます。
本プロジェクトでは、免疫抑制剤にかわり、移植された臓器に対する免疫反応だけを特異的に抑える細胞製品の開発を目指しています。この細胞製品により、臓器移植を受ける患者さんの移植後の生活にたくさんの笑顔をお届けできることを願っています。

免疫寛容とは
免疫反応を制御する細胞が、臓器移植のミライを変える
免疫反応は、感染症などから身を守る大切な反応ですが、自分の体の中に自分以外の存在を許さない、実はとてもわがままな反応です。 免疫細胞は体内に入ってきた異物を認識すると、たとえそれが体に必要なものであっても、そこに存在する理由などおかまいなしに攻撃します。移植された臓器は患者さんにとってとても大切なものですが、非常に大きな異物として激しい免疫反応(拒絶反応)を起こしてしまいます。しかし、一部の移植を受けた患者さんでは、免疫抑制剤の服用を止めても拒絶反応が起こっていないことが知られています。わがままな免疫細胞達が大きな異物のはずの他者の臓器が体内に存在することを許している状態は免疫寛容(トレランス)と呼ばれています。
私たちは、そのトレランスのメカニズム解明と、その過程で発見された、人為的に移植臓器に対するトレランスを誘導する治療法の開発を行っています。
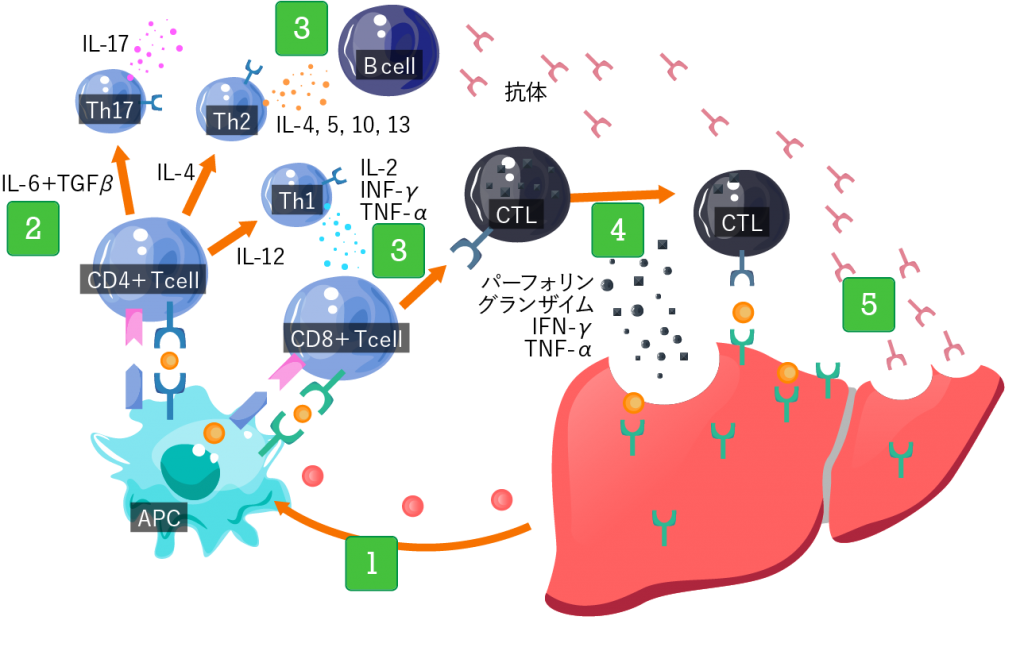
①拒絶反応
移植された臓器が、免疫細胞に異物(抗原)として認識されてしまうと、移植された臓器をターゲットにした免疫反応が起こります。攻撃を受けた移植臓器は、細胞が破壊され、そのままにしておくと消滅してしまいます。拒絶反応に関わっている免疫細胞は大きく分けて3種類(抗原提示細胞・T細胞・B細胞)あります。
- 抗原提示細胞(APC)が「異物」を自身の細胞内に取り込み(貪食)、それを細胞表面に提示して、攻撃ターゲットを他の免疫細胞に知らせます。
- ターゲットの提示を受けた一部のT細胞はヘルパーT細胞に変化します。
- ヘルパーT細胞は別のT細胞やB細胞を活性化します。
- 活性化したT細胞は細胞障害性T細胞(CTL)になり、直接ターゲットを攻撃します。
- 活性化したB細胞は、ターゲットに対する抗体を産生し攻撃します。
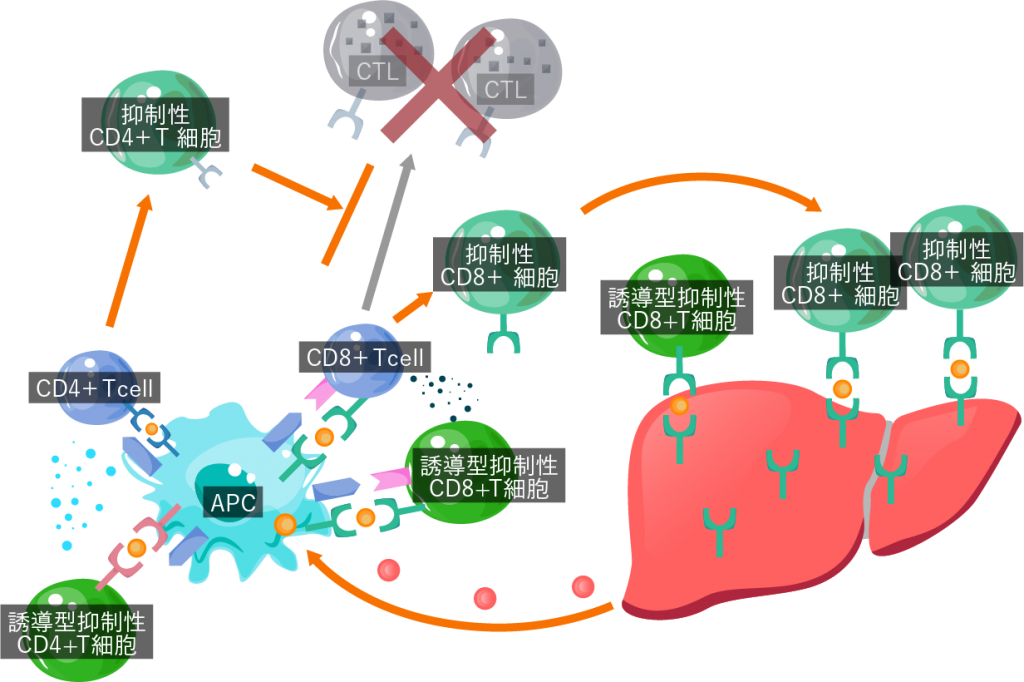
②免疫寛容
誘導型抑制性T細胞は、抗原提示細胞から示される特定のターゲットに対して、活性化を起こさないよう訓練された細胞です。移植臓器に対する拒絶反応は抑えつつ、病原体などへの反応には影響しないことが期待されています。
- 抗原提示細胞(APC)が「異物」を自身の細胞内に取り込み(貪食)、それを細胞表面に提示して、攻撃ターゲットを他の免疫細胞に知らせます。
- 特定のターゲットを提示している抗原提示細胞(APC)に、誘導型抑制性T細胞が結合します。
- もともと存在しているT細胞に働きかけ、同様の抑制能を持つ細胞に変化させます。
- 誘導型抑制性T細胞や、3の抑制能を獲得したT細胞が、ターゲットの細胞自体に結合し、細胞障害性T細胞(CTL)がその細胞に結合して攻撃するのを防ぎます。
![]()
誘導型抑制性T細胞とは
誘導型抑制性T細胞は、特定の抗原に対しての免疫反応を抑える働きを持つT細胞です。ドナーの方と患者さんの免疫細胞を体外に取り出し、免疫反応を抑える処理をして一緒に培養して作った、ドナーの臓器に対する免疫反応のみを終息させようとするT細胞です。
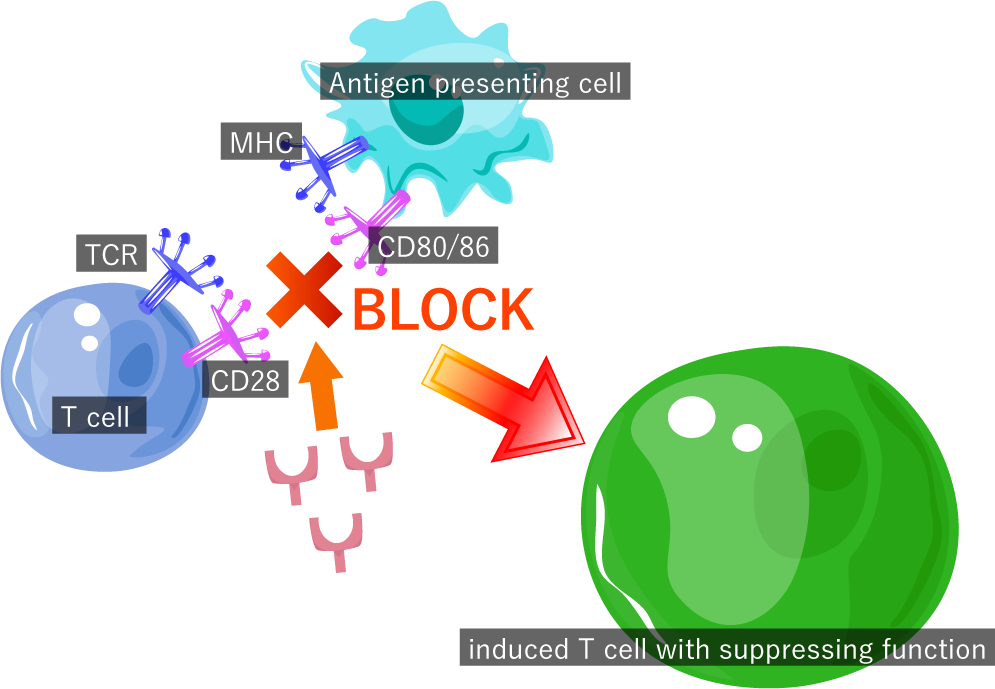
この抑制能を持つT細胞の作成には、抗CD80/86抗体を用います。CD80/86はT細胞表面のCD28に結合し、T 細胞が最初に活性化する時に、必要な共刺激を与えます。このCD80/86に抗体を結合させ、共刺激を遮断することで免疫反応を抑えます。
その結果、その抗原に対して免疫反応を起こさず、さらにはその抗原に対する免疫反応だけを抑制する細胞に変化します。
免疫寛容の仕組みについてもっとくわしく!
製品化に向けた取り組み
また、並行して安定した品質の細胞製品を患者さんのもとにお届けできるよう、製造方法の改良も目指しています。
誘導型抑制性T細胞は、免疫抑制剤にかわり移植された臓器に対する拒絶反応を特異的に抑え、高い有効性が期待される再生医療等製品の候補として、令和2年度 厚生労働省 先駆的医薬品等指定制度※対象品目に指定されています。
※画期性、対象としている疾患の重篤性、対象疾患に対する極めて高い有効性などの条件に合致する治験製品等を国が指定し、実用化に向けて優先的な取り扱いをする制度
製品開発のステップ
STEP1
基礎研究
誘導型抑制性T細胞の培養技術を開発 動物や細胞を用いた検討
STEP2
臨床研究
患者さんを対象とした効果・安全性の検討
STEP3
医師主導治験
患者さんを対象とした効果・安全性の検討を、国が定めたより厳しい規準下で実施中
(現在実施中の医師主導治験の対象:生体肝移植を受ける患者さん)
STEP4
国の承認
治験で得られたデータを国に提出し、承認を得ます
承認後は通常診療としてこの治療を多くの医療機関で受けられるようになります。
(STEP3の対象患者さんと同じ疾患の方のみです)
※臓器移植法が整備され移植医療は普及しつつありますが、脳死ドナーからの提供臓器は常に不足しており、特に肝臓・腎臓の移植については、患者さんのご家族から臓器の一部の提供を受ける生体移植の件数が脳死移植の件数を上回っています。今回の治験では、生体肝移植を受ける患者さんにご協力をお願いしています。今後は、他の疾患の患者さんを対象とした治験も実施する予定です。
製品化までの取り組みをもっとくわしく!
本プロジェクトの概要
本プロジェクトのはじまり
研究室から生まれた新規治療法
免疫は、病原体などから身体を守る大切なメカニズムです。しかし、免疫系が自己の細胞を異物とみなし過剰な反応を起こしてしまうことがあります。これが関節リウマチ、1型糖尿病、潰瘍性大腸炎などの自己免疫疾患です。一方で、反応する必要の無い異物に過剰に反応すると、食物アレルギーなどの、アレルギー疾患になります。
本プロジェクトの始まりは、1970年代に現免疫治療研究センター長の奥村先生とその師で当時既に著名な免疫学者であった故・多田富雄先生が、B細胞の抗体産生を抑制し免疫反応を終息させるT細胞の概念を提唱し、それをサプレッサーT細胞と呼んだことに遡ります。この免疫反応を終息させるT細胞の機能不全が自己免疫疾患の原因であり、そのメカニズムを解明できれば治療法の開発につながるのではないか。そして最も強い免疫反応である移植臓器への拒絶反応もこのサプレッサーT細胞で抑えることができるのではないか。
この免疫を抑制するシステムの研究は多くの研究者により続けられ、制御性T細胞と呼ばれる細胞が発見され注目を集めています。
本プロジェクトでは、抗CD80/86抗体を用いた、制御性T細胞を含む誘導型抑制性T細胞の製造方法を確立し、臨床応用を目指しています。
プロジェクトの背景
1963年、米コロラド大学において故トーマス・E・スターツル氏により世界初の肝臓移植が行われました。スターツル氏は、藤堂省元北海道大学教授ら多くの日本人医師を指導したことでも知られています。1968年に日本でも初の心臓移植術が行われました。が、この手術は後に各種の問題が提起され、日本の臓器移植は停滞してしまいます。臓器移植を実施するには、拒絶反応を抑える免疫抑制剤が必要です。日本では移植医療が停滞する一方で、1970年代に登場したシクロスポリン、1990年代に登場したタクロリムといった免疫抑制剤により、臓器移植の成績は飛躍的に向上します。
1980年代後半、日本においてもようやく臓器移植が実施される機運が生じ、1989年に国内で初めて行われた生体肝移植手術には承認前のタクロリムスが使用されました。1997年には臓器移植法が、2010年には改正法が施行され、日本でも臓器移植の件数は伸びてきましたが、まだまだ普及していないのが現状です。
免疫抑制剤により移植後早期に起こる激しい拒絶反応はほとんどみられなくなりました。移植後5年間患者さんが生存している割合は心臓、膵臓、腎臓で90%を超え、肝臓80%、肺、小腸は70%を超えています。
しかし、長期的な経過に目を向けると、必ずしも満足とは言えない状況です。この原因として、免疫抑制剤を長期間服用することによる副作用が挙げられます。
免疫反応を抑えることによる副作用として感染症・悪性腫瘍などがあります。新型コロナウイルスが話題になっていますが、免疫抑制剤服用中は、ワクチンを接種しても効果が得られにくいという報告もあり注意が必要です。また、高血圧や腎障害・肝障害、高血糖といった副作用も知られています。患者さんは副作用の治療薬も含めた多剤を服用することになり、併用薬の副作用や相互作用のリスク、感染を避けるための生活の制限、高血糖などのための食事制限に加え、高額な医療費の問題も積み重なります。
この問題を根本から解決するため、私たちは誘導型抑制性T細胞による移植片へのトレランス誘導を目指しています。この治療法を患者さんに届けるため、免疫学者と移植外科医が協力して研究を進めてきました。生体肝移植患者を対象とした最初の臨床試験は、北海道大学の藤堂省氏によって実施され、参加した10例の患者さんのうち7例の方が現在も免疫抑制剤を服用することなく過ごされています。
基礎研究グループ
抑制性免疫記憶と誘導型抑制性T細胞のメカニズム解明を目指して
誘導型抑制性T細胞と抑制性免疫記憶の関連、トレランスの誘導メカニズムについて研究しています。現在治験に参加いただいている生体肝移植を受ける患者さんだけではなく、他の臓器移植や脳死・死後移植を受ける患者さんにもこの治療法が応用できるか、また臓器移植のみならず、自己免疫疾患やアレルギー疾患などへもこの治療法が応用できるかも研究しています。
製造・品質管理グループ
誘導型抑制性T細胞の安定供給と効果のモニタリング方法確立を目指して
製品の製造とその品質チェックを担当する他、製品の効果をモニタリングする、リンパ球混合試験の確立を目指しています。
誘導型抑制性T細胞の製造とその品質チェックを担当しています。温度管理などが難しい生きた細胞から作られるこの製品を、安定した品質で全国の患者さんに届けられるよう製造や輸送過程の改良も目指しています。また、製品の効果をモニタリングする、B細胞を用いたリンパ球混合試験法の確立するための研究も行っています。
臨床(治験・臨床研究)グループ
誘導型抑制性T細胞の薬事承認を目指して
誘導型抑制性T細胞の薬事承認を目指し、治験・臨床研究を実施しています。
他大学病院で実施いただいている、患者さんを対象とした治験・臨床研究の代表機関として、研究計画を立案するとともに、製造チームと実施施設の調整やデータ収集状況の管理、当局対応などを担当しています。
研究者たちの取り組みをご紹介!
学会発表・論文
| 学会発表 |
|
|---|---|
| 論文 |
|
実用化を目指して
これからの研究課題
現在、これから生体肝移植を受ける患者さんを対象とした治験を実施中ですが、並行して下記の患者さんを対象とした研究も進めていきます。
・他の臓器の生体移植を受ける患者さん
・肝臓やその他の臓器の脳死/死後移植を受ける患者さん
・過去に臓器移植を受け、現在服用中の免疫抑制剤の副作用が問題となっている患者さん
・移植を受ける小児の患者さん
また、自己免疫疾患などへの臨床応用についても研究を進めています。

- トップページ
- 本プロジェクトのご紹介



